
Secciones
Servicios
Destacamos

marta castelló vellón
Valencia
Miércoles, 3 de febrero 2021, 10:59
La Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) ha publicado el primer informe de Farmacovigilancia sobre vacunas Covid-19 que recoge datos de los efectos secundarios notificados en España desde el 27 de diciembre de 2020 hasta el 12 de enero de 2021. ... Estos acontecimientos adversos han ocurrido en personas vacunadas con el fármaco autorizado en la Unión Europea Comirnaty (Pfizer-BioNTech) el 22 de diciembre de 2020.
De esta forma, el Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano (SEFV-H) ha recogido en su informe «cualquier problema de salud que ocurre después de la vacunación, sin que necesariamente tenga que estar ocasionado por la vacuna, ya que puede tratarse de problemas médicos que coinciden en el tiempo o que estén relacionados con el propio acto de la vacunación».
¿Dondé comprar mascarilas FFP2 baratas?
Noticia Relacionada
Hasta el día 12 de enero de 2021 se vacunaron un total de 494.799 personas, el 70% mujeres. En cuanto a la distribución por grupos de edad, el 62% corresponde a personas de entre 18 y 64 años y el 38% a mayores de 65 años, según el Registro de Vacunación del Ministerio de Sanidad.
En este periodo se han registrado un total de 374 notificaciones de acontecimientos adversos, lo que correspondería a 79 notificaciones por cada 100.000 personas vacunadas. El 91% han sido comunicadas por profesionales sanitarios, y el 9% por ciudadanos no profesionales sanitarios. La mayoría de los casos corresponden a mujeres (83%) y a personas de entre 18 y 64 años (67%).
Las 374 notificaciones incluyen 831 términos descriptores de acontecimientos adversos, ya que un mismo caso puede contener varios términos, por ejemplo, una persona puede haber presentado dolor en el lugar de inyección y fiebre tras la administración de la vacuna.
Noticia Relacionada
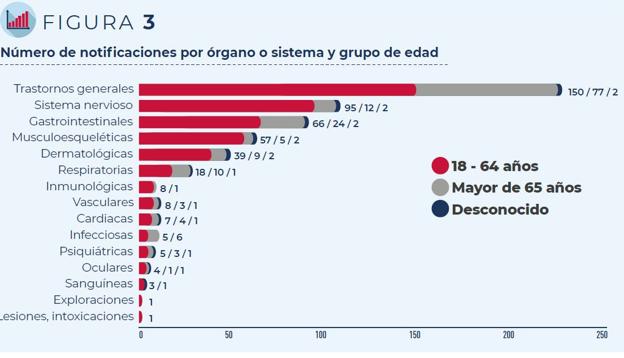
Los trastornos generales como fiebre o malestar general han sido los más frecuentemente notificados, seguidos de los trastornos del sistema nervioso (mayoritariamente cefaleas y mareos) y gastrointestinal (principalmente náuseas y diarrea), independientemente del grupo de edad o sexo de las personas vacunadas.
Con menos frecuencia se han reportado molestias musculoesqueléticas, dermatológicas y respiratorias, mientras los acontecimientos adversos respecto a problemas inmunológicos, vasculares, cardíacos, infecciosos, psiquiátricos, oculares y sanguíneos son muy poco habituales. Sólo se ha reportado un caso de posible intoxicación o lesión tras la vacunación.
A continuación se muestran un gráfico elaborado por la AEMPS de los principales efectos detectados según la edad de los pacientes:
La mayor atención en este periodo de tiempo ha estado centrada en los casos de anafilaxia, una reacción adversa conocida y referenciada en la ficha técnica y el prospecto de Comirnaty. Una revisión reciente del Center for Disease Control and Prevention de Estados Unidos estima una tasa de anafilaxia de 11.1 casos por millón de dosis administradas. En España, durante el periodo analizado en este informe, se han identificado 4 casos. Todos ellos ocurrieron en mujeres que se recuperaron o estaban en recuperación tras recibir el tratamiento correspondiente. En 3 de los casos constaban antecedentes personales de reacción alérgica.
Noticia Relacionada
La anafilaxia es una reacción alérgica grave muy poco frecuente que afecta simultáneamente a varios órganos, principalmente piel, sistema circulatorio y respiratorio. Los principales signos o síntomas incluyen urticaria o eritema generalizado, prurito generalizado con erupción, angioedema, hipotensión, taquicardia, disminución o pérdida de conciencia, sibilancias, estridor, inflamación de las vías respiratorias superiores o dificultad respiratoria. Generalmente aparece a los 15-30 minutos tras el contacto con el agente desencadenante y tiene una progresión rápida. Los síntomas pueden ser graves o amenazar la vida, por lo que es esencial el tratamiento inmediato con adrenalina.
La AEMPS recomienda no administrar una segunda dosis de la vacuna a aquellos pacientes que hayan presentado una reacción alérgica clínicamente relevante (anafilaxia, angioedema, urticaria generalizada, manifestaciones respiratorias, como asma o rinitis) tras recibir la primera dosis y derivar al paciente a un servicio de alergología para estudio.
¿Ya eres suscriptor/a? Inicia sesión
Publicidad
Publicidad
Te puede interesar
Publicidad
Publicidad
Esta funcionalidad es exclusiva para suscriptores.
Reporta un error en esta noticia
Comentar es una ventaja exclusiva para registrados
¿Ya eres registrado?
Inicia sesiónNecesitas ser suscriptor para poder votar.